「禁忌を含む注意事項等情報」等は電子添文をご参照ください。

一部用法・用量で定められた開始用量外の成績が含まれるが、承認時に評価されたデータのため掲載する。
第Ⅱ相臨床試験(用量反応試験)
試験概要
- 【 目 的 】 高リン血症を有する血液透析患者を対象として、ピートルの有効性用量反応性および安全性について、プラセボを対照とした二重盲検並行群間比較法により検討する。
- 【 対 象 】 高リン血症を有する血液透析中の慢性腎不全患者183例(FAS※:178例)
- 【 方 法 】3週間の観察期間(washout期間)後、ピートルチュアブル錠を750mg/日、1,500mg/日、2,250mg/日、3,000mg/日またはプラセボを1日3回、食直前に6週間経口投与した。
- 【試験デザイン】無作為化二重盲検プラセボ対照並行群間比較試験
- 【 有効性評価項目 】
- 主要評価項目:血清リン濃度(最終評価時における血清リン濃度の投与開始時からの変化量[検証的な解析項目]、測定値など)
副次評価項目:補正血清カルシウム濃度など
- 【安全性評価項目】副作用の発現状況など
有効性に関する主要評価項目は血清リン濃度、主要評価変数は最終評価時の血清リン濃度の変化量とした。主要評価変数は、群ごとに要約統計量(例数、平均値、SDなど)と平均値の両側95%信頼区間を求めた。また、群を固定効果、0週時の血清リン濃度を共変量とした共分散分析を行い、プラセボに対する優越性を検討した。その他、群ごとに各評価時期における血清リン濃度の要約統計量を算出した。安全性について、副作用は群ごとに発現例数および発現率を求めた。
- ※
- FAS(Full Analysis Set):最大の解析対象集団。GCP違反例、未投薬例、治療期移行前中止例、不適格例の一部の症例および主要評価項目が得られていない症例を除外した集団。
- 6.
- 用法及び用量
通常、成人には、鉄として1回250mgを開始用量とし、1日3回食直前に経口投与する。以後、症状、血清リン濃度の程度により適宜増減するが、最高用量は1日3000mgとする。
- 7.
- 用法及び用量に関連する注意(抜粋)
- 7.2
- 増量を行う場合は、増量幅を鉄として1日あたりの用量で750mgまでとし、1週間以上の間隔をあけて行うこと
ピートルの血清リン濃度低下作用– 第Ⅱ相臨床試験(用量反応試験)-
承認時評価資料:国内第Ⅱ相臨床試験(PA1201)/Koiwa F et al.;Clin Exp Nephrol. 2017; 21: 513-522.(この試験はキッセイ薬品工業株式会社の支援により実施された)
血清リン濃度の推移
(主要評価項目)
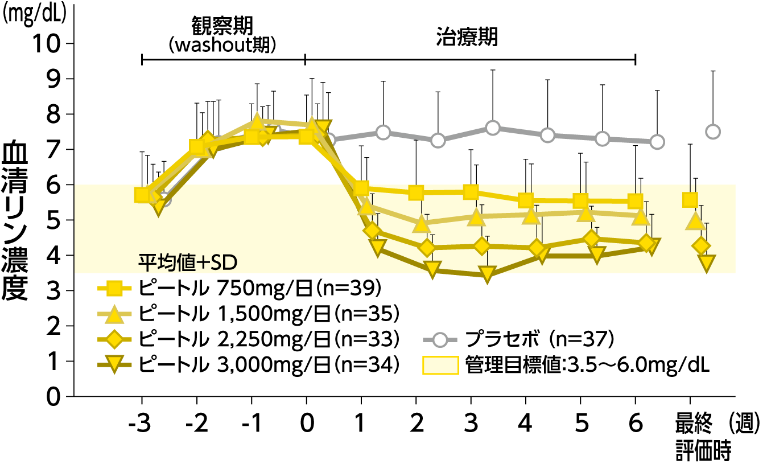
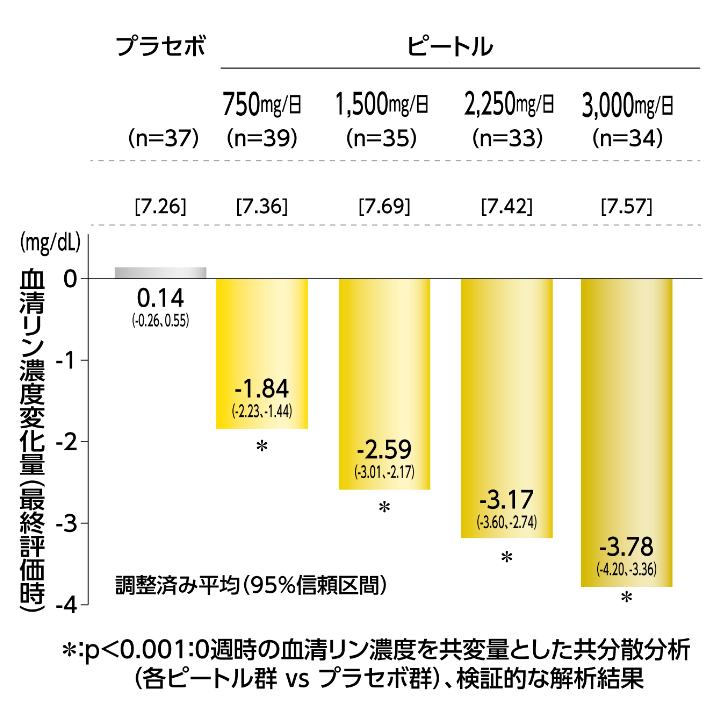
血清リン濃度の変化量
(主要評価項目[検証的な解析結果])
安全性: 副作用
副作用発現率はピートル750mg/日群は23.1%(9/39例)、1,500mg/日群は13.9%(5/36例)、2,250mg/日群は40.0%(14/35例)、3,000mg/日群は44.4%(16/36例)、プラセボ群は10.8%(4/37例)でした。ピートル群の主な副作用は下痢で750mg/日群は10.3%(4/39例)、1,500mg/日群は11.1%(4/36例)、2,250mg/日群は34.3%(12/35例)、3,000mg/日群は33.3%(12/36例)でした。 プラセボ群の主な副作用は下痢8.1%(3/37例)、鼓腸5.4%(2/37例)でした。 なお、本試験において重篤な副作用は認められませんでした。投与中止に至った副作用として、ピートル1,500mg/日群において下痢が2例、2,250mg/日群において下痢が5例、便秘が1例、3,000mg/日群において下痢が4例、腹部膨満が1例、心窩部不快感が1例に認められました。
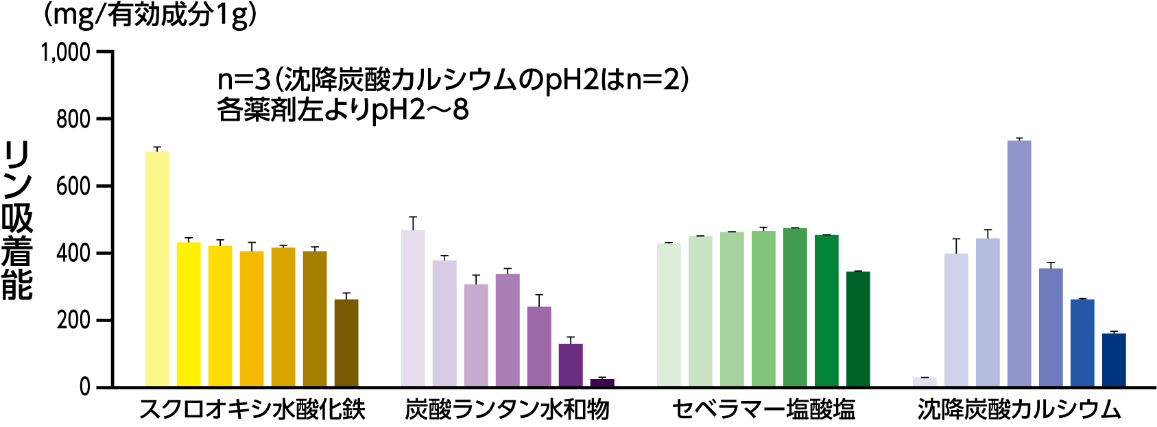
各リン吸着薬のリン吸着能(in vitro)
Yaguchi A, et al.: BMC Nephrol. 2019; 20: 465. より改変 (本試験はキッセイ薬品工業株式会社の資金提供により実施された。著者は全員キッセイ薬品工業株式会社の社員である。)
pH2、3、4、5、6、7、8において、各リン吸着薬のリン吸着能(有効成分1gあたりが吸着したリン酸塩の量)を測定しました。
その結果、スクロオキシ水酸化鉄はいずれのpHでもリン吸着能が示されました。
【目 的】
リン吸着薬の有効性を評価するため、試験として消化管内のpHを模した溶液を用いて、各リン吸着薬(スクロオキシ水酸化鉄、炭酸ランタン水和物、セベラマー塩酸塩および沈降炭酸カルシウム)のリン吸着能を検討する。
【方 法】
消化管内の状態を模擬したpH2~8に調整したリン酸塩溶液(40mL、20mM)に各リン吸着薬200mgを加えて撹拌(37℃、2時間)および遠心分離(37℃、2,330×g、5分)した後、上澄み液中のリン濃度を測定した。本試験では各リン吸着薬の有効成分をそれぞれの金属またはセベラマーとし、各有効成分1gに吸着されたリン酸塩の量をリン吸着能とした。

効能又は効果、用法及び用量、禁忌を含む注意事項情報等については、各製品の電子添文をご覧ください。